![]()
![]() Abychom se dověděli co nejvíce o automobilových palivech a emisích, navštívili jsme Ústav technologie ropy a petrochemie , který je součástí fakulty technologie ochrany prostředí. Tato fakulta je jednou ze 4 fakult Vysoké školy chemicko technologické v Praze. Ústav úzce spolupracuje s rafinériemi ropy i s automobilovým průmyslem a výzkumnými ústavy. Řeší se zde právě vztah mezi složením paliv a emisemi, zejména se sledují polyaromatické uhlovodíky a aldehydy, tj. složky, pro něž zatím nejsou stanoveny limity. Dověděli jsme se mnoho zajímavého, získali jsme kopie výzkumných zpráv a článků pro odborné časopisy. Ty jsme si pak rozdělili k prostudování.
Abychom se dověděli co nejvíce o automobilových palivech a emisích, navštívili jsme Ústav technologie ropy a petrochemie , který je součástí fakulty technologie ochrany prostředí. Tato fakulta je jednou ze 4 fakult Vysoké školy chemicko technologické v Praze. Ústav úzce spolupracuje s rafinériemi ropy i s automobilovým průmyslem a výzkumnými ústavy. Řeší se zde právě vztah mezi složením paliv a emisemi, zejména se sledují polyaromatické uhlovodíky a aldehydy, tj. složky, pro něž zatím nejsou stanoveny limity. Dověděli jsme se mnoho zajímavého, získali jsme kopie výzkumných zpráv a článků pro odborné časopisy. Ty jsme si pak rozdělili k prostudování.
![]() Málokdo si uvědomuje, že ovzduší je znečišťováno uhlovodíky (dále HC) v důsledku odpařování benzinů z palivového systému automobilů, během jejich provozu a stání a při tankování a přečerpávání paliva. Tyto emise samozřejmě odpovídají složení paliva a těkavosti jeho složek. Jsou pochopitelně tím větší, čím je vyšší teplota. Množství HC ve výfukových plynech ku množství HC unikajících do ovzduší odparem je zhruba 5 : 3.
Málokdo si uvědomuje, že ovzduší je znečišťováno uhlovodíky (dále HC) v důsledku odpařování benzinů z palivového systému automobilů, během jejich provozu a stání a při tankování a přečerpávání paliva. Tyto emise samozřejmě odpovídají složení paliva a těkavosti jeho složek. Jsou pochopitelně tím větší, čím je vyšší teplota. Množství HC ve výfukových plynech ku množství HC unikajících do ovzduší odparem je zhruba 5 : 3.
![]() Opatření pro snížení těchto emisí
Opatření pro snížení těchto emisí
![]() Rafinérie snižují obsah nejtěkavějších uhlovodíků - tedy C4 frakce. Tyto složky se v minulosti uplatňovaly jako vysokooktanové podíly benzinového poolu.
Rafinérie snižují obsah nejtěkavějších uhlovodíků - tedy C4 frakce. Tyto složky se v minulosti uplatňovaly jako vysokooktanové podíly benzinového poolu.
![]() Nové automobily jsou již standardně vybavovány (v západní Evropě od 1. 1. 1993) přídavnými nádržemi s aktivním uhlím - tzv. Carbon Canister (CC), na němž se vypařené HC nejprve adsorbují a v regenerativní fázi zvýšenou teplotou desorbují do sání běžícího motoru. Je-li kapacita adsorbéru dostatečná - tzv. Large Carbon Canister (LCC), zachycují se účinně i výpary při tankování (asi 1,3 g benzinu na každý litr). Lokální koncentrace HC u čerpacích stojanů jsou velmi vysoké a ohrožují především zdraví personálu.
Nové automobily jsou již standardně vybavovány (v západní Evropě od 1. 1. 1993) přídavnými nádržemi s aktivním uhlím - tzv. Carbon Canister (CC), na němž se vypařené HC nejprve adsorbují a v regenerativní fázi zvýšenou teplotou desorbují do sání běžícího motoru. Je-li kapacita adsorbéru dostatečná - tzv. Large Carbon Canister (LCC), zachycují se účinně i výpary při tankování (asi 1,3 g benzinu na každý litr). Lokální koncentrace HC u čerpacích stojanů jsou velmi vysoké a ohrožují především zdraví personálu.
![]() I složení těchto emisí je ovlivněno složením paliva, i když zde hraje velkou roli konstrukce motoru a režim spalování. Výrobci paliv i automobilů jsou stále více pod tlakem legislativních opatření nuceni přispívat ke zmenšování negativního vlivu automobilů na kvalitu ovzduší.
I složení těchto emisí je ovlivněno složením paliva, i když zde hraje velkou roli konstrukce motoru a režim spalování. Výrobci paliv i automobilů jsou stále více pod tlakem legislativních opatření nuceni přispívat ke zmenšování negativního vlivu automobilů na kvalitu ovzduší.
![]() Hlavní složky: CO2, H2O (g), N2 - relativně neškodné
Hlavní složky: CO2, H2O (g), N2 - relativně neškodné
![]() Škodlivé složky:
Škodlivé složky:
a) Složky, jejichž obsah je legislativně stanoven, tj. CO, NOx, HC někdy HCHO. Pojem uhlovodíky zahrnuje jak nespálené uhlovodíky z paliva, tak uhlovodíky nově vzniklé během spalovacího procesu.
b) Složky, jejichž obsah není dosud legislativně stanoven, ale jsou sledovány z hlediska jejich škodlivého vlivu na živé organismy. Jsou to zejména benzen, 1,3-butadien, polyaromatické uhlovodíky (dále PAU), nitrované PAU, dále formaldehyd, acetaldehyd. Obsahy PAU a N-PAU jsou sice velmi nízké (a proto je jejich stanovení náročné a složité), ale stupeň zdravotní rizikovosti je velmi vysoký. Lze však očekávat, že brzo budou stanoveny limity i na některé z těchto látek.
c) U olovnatých benzinů přicházejí navíc v úvahu emise Pb v různé formě. Dnes se již upouští od přídavků alkylhalogenidů jako vynašečů olova, takže Pb, které bylo dříve emitováno jako PbCl2 nebo PbBr2 se vyskytuje v jiných formách - PbO, Pb3O4, případně jako PbSO4, neboť palivo obsahuje i velmi malé procento síry (pod 0,005%). Tyto formy jsou méně těkavé a méně rozpustné.
![]() Pro ilustraci pestrého složení emisí uvádíme přehled sloučenin identifikovaných při stanovení těkavých HC (tabulka 1, str. 26) a přehled identifikovaných PAU (tabulka 2, str.26) v emisích zážehových motorů. Údaje jsou převzaty z výzkumné zprávy "Vypracování metodiky stanovení organických látek ve výfukových plynech ze spalování automobilových benzinů" - Ústav ropy a petrochemie VŠCHT.
Pro ilustraci pestrého složení emisí uvádíme přehled sloučenin identifikovaných při stanovení těkavých HC (tabulka 1, str. 26) a přehled identifikovaných PAU (tabulka 2, str.26) v emisích zážehových motorů. Údaje jsou převzaty z výzkumné zprávy "Vypracování metodiky stanovení organických látek ve výfukových plynech ze spalování automobilových benzinů" - Ústav ropy a petrochemie VŠCHT.
![]() Složení výfukových plynů u vznětových motorů
Složení výfukových plynů u vznětových motorů
![]() Emise základních škodlivin (bod a) jsou podstatně menší, zato jsou vyšší emise tuhých částic, především sazí, na nichž se adsorbují velmi škodlivé PAU. Mimoto je v palivu nezanedbatelný obsah síry (evropská norma EN 590 od 1. 10. 1996 povoluje max. 0,05%), která je emitována jako SO2.
Emise základních škodlivin (bod a) jsou podstatně menší, zato jsou vyšší emise tuhých částic, především sazí, na nichž se adsorbují velmi škodlivé PAU. Mimoto je v palivu nezanedbatelný obsah síry (evropská norma EN 590 od 1. 10. 1996 povoluje max. 0,05%), která je emitována jako SO2.


![]() Rozsah mezi minimální a maximální hodnotou emise pokrývá rozdíly v obsahu škodlivin u různých tipů a velikostí motorů.
Rozsah mezi minimální a maximální hodnotou emise pokrývá rozdíly v obsahu škodlivin u různých tipů a velikostí motorů.
Tabulka 1
n-Alkany
|
Propan |
butan |
pentan |
hexan |
heptan |
oktan |
nonan |
i-Alkany
|
2-methylpropan |
2-methylbutan |
2,3-dimethylbutan |
2-methylpentan |
3-methylpentan |
|
2,2-dimethylpentan |
2,4-dimethylpentan |
3,3-dimethylpentan |
3-ethylpentan |
3-methylhexan |
|
2-methylhexan |
2,2-dimethylhexan |
2,5-dimethylhexan |
2,4-dimethylhexan |
3,3-dimethylhexan |
|
2,3-dimethylhexan |
2-methylheptan |
4-methylheptan |
3,4-dimethylhexan |
3-methylheptan |
|
2,2-dimethylheptan |
2,4-dimethylheptan |
3,3-dimethylheptan |
4-ethylheptan |
4-methyloktan |
|
2-methyloktan |
3-ethylheptan |
3-methyloktan |
C10-isoalkany |
C11- isoalkany |
Cykloalkany
|
Cyklopentancyklohexan |
1,1-dimethylcyklopentan |
|||
|
1,3-dimethylcyklopentan |
1,2-dimethylcyklopentan |
Methylcyklohexan |
1,1,3-trimethylcyklopent. |
|
|
Ethylcyklopentan |
1,2,4-trimethylcyklopent. |
1,2,3-trimethylcyklopent. |
1,1,2-trimethylcyklopent. |
|
|
1,3-dimethylcyklohexan |
1,4-dimethylcyklohexan |
1,1-dimethylcyklohexan |
3-ethyl-1- methylcyklopent. |
|
|
2-ethyl-1-methylcyklopent |
1-ethyl-1- ethylcyklopent |
1,2-dimethylcyklohexan |
1,1,4-trimethylcyklohexan |
|
|
Alkylcyklopentany C9 -C11 |
alkylcyklohexany C9 -C11 |
|||
Aromáty
|
benzen |
Toluen |
m-xylen |
p-xylen |
|
o-xylen |
i-propylbenzen |
propylbenzen |
1-ethyl-3-methylbenzen |
|
1-ethyl-4-methylbenzen |
1,3,5-trimethylbenzen |
1-ethyl-2-methylbenzen |
1,2,4-trimethylbenzen |
|
i-butylbenzen |
1,2,3-trimethylbenzen |
indan |
methylindan |
|
C4-alkylbenzeny |
C5-alkylbenzeny |
naftalen |
1-methylnaftalen |
|
2-methylnaftalen |
Alkeny
|
1-buten |
2-buten |
2-methylpropen |
3-methyl-1-buten |
1-penten |
|
2-methyl-1-buten |
2-penten |
2-methyl-2-buten |
cyklopenten |
4-methyl-1-penten |
|
3-methyl-1-penten |
2-methyl-1-penten |
1-hexen |
3-hexen |
2-hexen |
|
2-methyl-2-penten |
3-methyl-2-penten |
Dimethylpenteny |
methylhexeny |
Ethylpenten |
|
styren |
Methylstyren |
Kyslíkaté sloučeniny
methyl-t-butylether
Tabulka 2
|
Fluoren |
C1 - C2 alkylfluoreny |
Fenanthren |
C1 - C4 fenanthreny |
|
Anthracen |
C1 - C2 alkylanthraceny |
Fluoranthen |
Methylfluorantheny |
|
Pyren |
C1 - C3 alkylpyreny |
Chrysen |
benzo [ b] fluoranthen |
|
benzo[k]fluoranthen |
benzo [ e] pyren |
benzo [ a] pyren |
benzo [ ghi] perylen |
|
dibenzo [ e,l] pyren |
koronen |
![]() Na závěr tohoto přehledu o složení emisí bychom chtěli upozornit na skutečnost, kterou si lidé příliš neuvědomují. Při spalování jakéhokoli paliva se spotřebovává kyslík a vzniká nejedovatý oxid uhličitý. Jenže obsah CO2 v atmosféře povážlivě vzrůstá a je známo, že CO2 spolu s některými dalšími plyny způsobuje tzv. skleníkový efekt. Vědci ještě nejsou zajedno, zda nastane globální oteplování, které by mělo pro lidstvo katastrofální následky, ale je rozhodně jisté, že přírodní rovnováha je vlivem spalovacích procesů narušena. O aktuálnosti problému svědčí i konání mezinárodní konference o emisích CO2 v japonském Kjótu v prosinci 1997.
Na závěr tohoto přehledu o složení emisí bychom chtěli upozornit na skutečnost, kterou si lidé příliš neuvědomují. Při spalování jakéhokoli paliva se spotřebovává kyslík a vzniká nejedovatý oxid uhličitý. Jenže obsah CO2 v atmosféře povážlivě vzrůstá a je známo, že CO2 spolu s některými dalšími plyny způsobuje tzv. skleníkový efekt. Vědci ještě nejsou zajedno, zda nastane globální oteplování, které by mělo pro lidstvo katastrofální následky, ale je rozhodně jisté, že přírodní rovnováha je vlivem spalovacích procesů narušena. O aktuálnosti problému svědčí i konání mezinárodní konference o emisích CO2 v japonském Kjótu v prosinci 1997.
![]() Jednoduchý výpočet, při němž zanedbáme nedokonalost spalování a nebudeme počítat s obsahem kyslíkatých složek v palivu, nám ukáže, kolik kyslíku nám automobily berou a kolik CO2 produkují.
Jednoduchý výpočet, při němž zanedbáme nedokonalost spalování a nebudeme počítat s obsahem kyslíkatých složek v palivu, nám ukáže, kolik kyslíku nám automobily berou a kolik CO2 produkují.
![]() Zadání úlohy :
Zadání úlohy :
![]() Na ujetí 100 km spotřebuje automobil 7,0 dm3 benzinu. Vypočtěte, kolik O2 spotřebuje a kolik CO2 vyprodukuje, za předpokladu úplného spálení na těchto 100 km. Počítejme s hustotou benzinu 730 kg.m-3 a elementárním složením 89% C a 11% H (hmot%).
Na ujetí 100 km spotřebuje automobil 7,0 dm3 benzinu. Vypočtěte, kolik O2 spotřebuje a kolik CO2 vyprodukuje, za předpokladu úplného spálení na těchto 100 km. Počítejme s hustotou benzinu 730 kg.m-3 a elementárním složením 89% C a 11% H (hmot%).
![]() Řešení :
Řešení :
C + O2 ® CO2
4 H + O2 ® 2 H2O
![]() Hmotnost benzinu m = 7,0 dm3 * 0,730 kg.dm-3 = 5,11 kg
Hmotnost benzinu m = 7,0 dm3 * 0,730 kg.dm-3 = 5,11 kg
![]() Hmotnost C mC = 0,89 * 5,11 kg
Hmotnost C mC = 0,89 * 5,11 kg
![]() Hmotnost H mH = 0,11 * 5,11 kg
Hmotnost H mH = 0,11 * 5,11 kg
![]() Látkové množství C nC = 0,89 * 5,11 kg / 0,012 kg.mol-1 = 379 mol
Látkové množství C nC = 0,89 * 5,11 kg / 0,012 kg.mol-1 = 379 mol
![]() Látkové množství H nH = 0,11 * 5,11 kg/ 0,001 kg.mol-1 = 562 mol
Látkové množství H nH = 0,11 * 5,11 kg/ 0,001 kg.mol-1 = 562 mol
![]() Z rovnic je patrno, že nCO2 = nC a nO2 = nC + 1/4 nH
Z rovnic je patrno, že nCO2 = nC a nO2 = nC + 1/4 nH
![]() Vznikne tedy 379 mol CO2 a spotřebuje se (379 + 562/4) mol = 519,5 mol O2
Vznikne tedy 379 mol CO2 a spotřebuje se (379 + 562/4) mol = 519,5 mol O2
![]() Hmotnost vzniklého CO2 mCO2 = 379 mol * 0,044 kg.mol-1 = 16,7 kg
Hmotnost vzniklého CO2 mCO2 = 379 mol * 0,044 kg.mol-1 = 16,7 kg
![]() Hmotnost spotřebovaného O2 mO2 = 519,5 mol * 0,032 kg.mol-1 = 16,6 kg
Hmotnost spotřebovaného O2 mO2 = 519,5 mol * 0,032 kg.mol-1 = 16,6 kg
![]() Výsledek nás docela překvapil. Asi budeme v budoucnu více chodit pěšky nebo jezdit na kole.
Výsledek nás docela překvapil. Asi budeme v budoucnu více chodit pěšky nebo jezdit na kole.
![]() Důležitý je zde tlak ze strany státních orgánů, ekologů a veřejnosti, který vyúsťuje ve stále se zpřísňující limity emisí. Iniciativa snižování vlivu motorových vozidel na životní prostředí vyšla z USA, kde jsou nejpřísnější předpisy v Kalifornii. Pozadu nezůstává Japonsko a Kanada. Země západní Evropy zavádějí přísnější limity s několikaletým zpožděním vůči USA. Země střední a východní Evropy se musí velmi rychle těmto trendům přizpůsobovat.
Důležitý je zde tlak ze strany státních orgánů, ekologů a veřejnosti, který vyúsťuje ve stále se zpřísňující limity emisí. Iniciativa snižování vlivu motorových vozidel na životní prostředí vyšla z USA, kde jsou nejpřísnější předpisy v Kalifornii. Pozadu nezůstává Japonsko a Kanada. Země západní Evropy zavádějí přísnější limity s několikaletým zpožděním vůči USA. Země střední a východní Evropy se musí velmi rychle těmto trendům přizpůsobovat.
![]() Tlak legislativy je vyvíjen dvěma směry :
Tlak legislativy je vyvíjen dvěma směry :
![]() 1) na složení paliv a tedy na rafinerie
1) na složení paliv a tedy na rafinerie
![]() 2) na výrobce automobilů
2) na výrobce automobilů
![]() Opatření rafinérií
Opatření rafinérií
![]() Opatření výrobců automobilů
Opatření výrobců automobilů
![]() Katalytické konvertory výfukových plynů
Katalytické konvertory výfukových plynů
![]() Používání katalytických konvertorů se nejprve rozšířilo v USA (od r. 1975), pak v Kanadě a Japonsku. V zemích EU se začaly konvertory používat v 80. letech. Od 1. 1. 1993 jsou jimi standardně vybaveny všechny vyráběné automobily (i v ČR). Vývoj katalytických konvertorů dospěl k řízeným trojcestným katalyzátorům. Jsou to katalyzátory, které jsou schopné přeměňovat současně CO, HC a NOx. Přitom probíhají simultánně tyto hlavní reakce:
Používání katalytických konvertorů se nejprve rozšířilo v USA (od r. 1975), pak v Kanadě a Japonsku. V zemích EU se začaly konvertory používat v 80. letech. Od 1. 1. 1993 jsou jimi standardně vybaveny všechny vyráběné automobily (i v ČR). Vývoj katalytických konvertorů dospěl k řízeným trojcestným katalyzátorům. Jsou to katalyzátory, které jsou schopné přeměňovat současně CO, HC a NOx. Přitom probíhají simultánně tyto hlavní reakce:
![]()
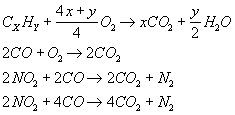
![]() Redukce NOx a oxidace CO jsou vzájemně vázány. Na obsahu kyslíku jsou závislé všechny reakce. Poměr množství kyslíku ve spalinách skutečně přítomného ku množství, které by bylo potřebné k úplné přeměně se označuje jako hodnota l.
Redukce NOx a oxidace CO jsou vzájemně vázány. Na obsahu kyslíku jsou závislé všechny reakce. Poměr množství kyslíku ve spalinách skutečně přítomného ku množství, které by bylo potřebné k úplné přeměně se označuje jako hodnota l.
![]() Oxidační reakce probíhají tím lépe, čím je kyslíku více (chudá směs) tj. l > 1. Na redukci NOx se pak nedostává CO. Naopak u bohaté směsi (l < 1) se pro nedostatek kyslíku oxidují jen malá množství CO a HC, ale stupeň přeměny NOx je vysoký. Optimálního stupně přeměny u všech škodlivin se dosahuje v úzkém rozmezí kolem hodnoty l = 1.
Oxidační reakce probíhají tím lépe, čím je kyslíku více (chudá směs) tj. l > 1. Na redukci NOx se pak nedostává CO. Naopak u bohaté směsi (l < 1) se pro nedostatek kyslíku oxidují jen malá množství CO a HC, ale stupeň přeměny NOx je vysoký. Optimálního stupně přeměny u všech škodlivin se dosahuje v úzkém rozmezí kolem hodnoty l = 1.
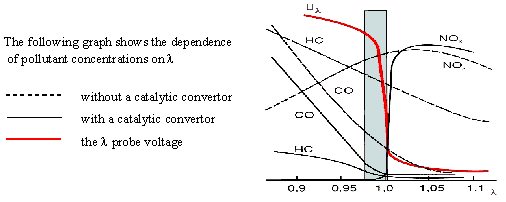
![]() Proto je před katalyzátor zařazena tzv. l sonda, což je elektrochemické čidlo, které měří obsah kyslíku před katalyzátorem a signál se používá k elektronickému ovládání přípravy palivové směsi. l sonda je v principu koncentrační článek s pevným elektrolytem ZrO2, elektrody jsou platinové. Napětí se řídí Nernstovou rovnicí:
Proto je před katalyzátor zařazena tzv. l sonda, což je elektrochemické čidlo, které měří obsah kyslíku před katalyzátorem a signál se používá k elektronickému ovládání přípravy palivové směsi. l sonda je v principu koncentrační článek s pevným elektrolytem ZrO2, elektrody jsou platinové. Napětí se řídí Nernstovou rovnicí:
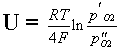 | |
![]() Katalytický konvertor se skládá z keramického nosiče s mnoha kanálky, na jehož povrch je nanesen vlastní katalyzátor. Dnes se užívají buď platinové kovy Pt, Rh, Pd (Pt : Rh je obvykle 1:5) nebo katalyzátory na bázi oxidů (NiO, Cr2O3, CuO, MnO2).
Katalytický konvertor se skládá z keramického nosiče s mnoha kanálky, na jehož povrch je nanesen vlastní katalyzátor. Dnes se užívají buď platinové kovy Pt, Rh, Pd (Pt : Rh je obvykle 1:5) nebo katalyzátory na bázi oxidů (NiO, Cr2O3, CuO, MnO2).
![]() V současné době dokáže nový katalytický konvertor v optimálním režimu odstranit škodliviny z 95 - 98 %. Problémem zůstává jeho malá účinnost při nízkých teplotách (studené starty). To se dá řešit např. elektrickým vyhříváním konvertoru a recyklací spalin. Konverzní schopnost katalyzátorů postupně při provozu klesá. Pokud nedojde k otrávení nebo k extrémnímu přehřátí katalyzátoru, zaručují výrobci vyhovující účinnost do 100 000 km.
V současné době dokáže nový katalytický konvertor v optimálním režimu odstranit škodliviny z 95 - 98 %. Problémem zůstává jeho malá účinnost při nízkých teplotách (studené starty). To se dá řešit např. elektrickým vyhříváním konvertoru a recyklací spalin. Konverzní schopnost katalyzátorů postupně při provozu klesá. Pokud nedojde k otrávení nebo k extrémnímu přehřátí katalyzátoru, zaručují výrobci vyhovující účinnost do 100 000 km.
![]() Pro katalyzátory na bázi platinových kovů jsou katalytickými jedy především olovo, fosfor, síra a některé konstrukční kovy. V ČR je hlavním problémem Pb (norma pro bezolovnatý benzin připouští 0,013 g Pb/l). Zdrojem fosforu jsou aditiva mazacích olejů.
Pro katalyzátory na bázi platinových kovů jsou katalytickými jedy především olovo, fosfor, síra a některé konstrukční kovy. V ČR je hlavním problémem Pb (norma pro bezolovnatý benzin připouští 0,013 g Pb/l). Zdrojem fosforu jsou aditiva mazacích olejů.